Page 48 - bingx
P. 48
1. KEGIATAN BELAJAR II
1.1. KD DAN IPK
Kompetensi Dasar (KD) Indikator Pencapaian Kompetensi (IPK)
3.3. Menganalisis 3.5.1 Menjelaskan prinsip dan aturan penulisan
struktur atom konfigurasi elektron
berdasarkan teori 3.5.2 Menuliskan konfigurasi elektron dalam
atom Bohr dan bentuk diagram orbital
teori mekanika 3.5.3 Menentukan bilangan kuantum dari setiap
kuantum. elektron.
4.3.Mengolah dan 4.5.1 Melaporkan hasil diskusi struktur atom
menganalisis truktur berdasarkan teori atom Bohr dan mekanika
atom berdasarkan teori kuantum
atom Bohr dan teori
mekanika kuantum.
1.2. MATERI
A. Struktur Atom Bohr
Masih ingatkah kalian dengan model atom yang dikemukakan oleh Ernest
Rutherford (1871–1937). Menurut Rutherford, atom terdiri dari inti yang bermuatan positif
dan dikelilingi elektron yang bermuatan negatif. Namun, jika suatu partikel yang bermuatan
listrik bergerak melingkar akan mengemisikan energinya dalam bentuk cahaya yang
mengakibatkan percepatan partikel semakin berkurang dan akhirnya diam. Dengan
demikian, jika elektron yang bermuatan negatif bergerak melingkar (mengelilingi inti
bermuatan positif) maka akan kehilangan energinya sehingga gerakan elektron akan
berkurang, yang akhirnya akan jatuh ke inti. Namun pada kenyataannya, elektron tidak
jatuh ke inti. Rutherford tidak mampu menjelaskan mengapa elektron tidak dapat jatuh ke
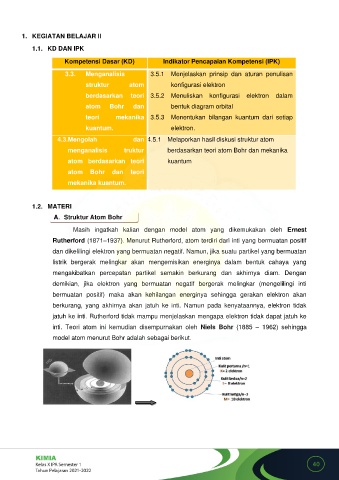
inti. Teori atom ini kemudian disempurnakan oleh Niels Bohr (1885 – 1962) sehingga
model atom menurut Bohr adalah sebagai berikut.
40