Page 103 - bingx
P. 103
3. KEGIATAN BELAJAR III
3.1 KD DAN IPK
Kompetensi Dasar (KD) Indikator Pencapaian Kompetensi (IPK)
3.7 Menganalisis teori jumlah 3.7.1 Menjelaskan tiga prinsip dasar teori domain
pasangan elektron di sekitar elektron
inti atom (Teori Domain 3.7.2 Menentukan jumlah domain elektron dari
Elektron) untuk menentukan struktur Lewis senyawa
bentuk molekul. 3.7.3 Menganalisis jumlah dan jenis pasangan
elektron untuk menentukan bentuk molekul
senyawa
4.7 Meramalkan bentuk molekul 4.7.1. Meramalkan bentuk molekul senyawa
berdasarkan teori jumlah tersebut berdasarkan teori domain elektron
pasangan elektron di sekitar dengan tahapan yang benar
inti atom (Teori Domain 4.7.2. Membuat bentuk molekul sederhana
Elektron). menggunakan plastisin dan sapu lidi
dengan benar
3.2 MATERI
a. Uraian Materi
Kepolaran Senyawa
Ikatan kovalen adalah ikatan yang terjadi antara unsur nonlogam dengan unsur nonlogam
yang lain dengan cara pemakaian bersama pasangan elektron.
Polarisasi Ikatan Kovalen
Suatu senyawa tersusun dari dua atau lebih atom. Setiap unsur memiliki harga
keelektronegatifan yang berbeda-beda. Perbedaan keelektronegatifan ini terjadi karena perbedaan
jari-jari, energy ionisasi, dan afinitas suatu unsur.
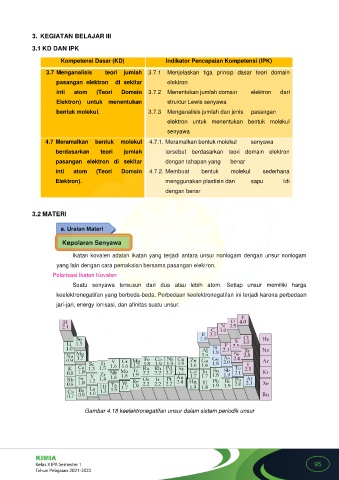
Gambar 4.18 keelektronegatifan unsur dalam sistem periodik unsur
95