Page 105 - bingx
P. 105
2) Bentuk molekul
Pada umumnya, jika bentuk molekul suatu senyawa simetris maka senyawanya bersifat
nonpolar, sedangkan jika bentuk molekulnya tidak simetris maka senyawanya bersifat polar.
Momen dipol (µ) merupakan jumlah vektor dari momen ikatan dan momen pasangan elektron
bebas dalam suatu molekul. Momen ikatan mempunyai arah dari muatan parsial positif ke
muatan parsial negatif. Molekul dikatakan bersifat polar jika memiliki µ > 0 atau µ ≠ 0 dan
dikatakan bersifat nonpolar jika memiliki µ = 0 .
Molekul yang
memiliki atom yang sama
seperti Cl2, Br2, I2, dan H2
bersifat nonpolar karena
molekul tersebut tidak
memiliki momen ikatan
maupun momen pasangan
elektron bebas (PEB)
sehingga momen dipolnya
bernilai 0. Tidak hanya
molekul dengan atom-
atom yang sama, pada
molekul yang memiliki atom-atom yang berbeda pun dapat bersifat nonpolar. Misalnya pada
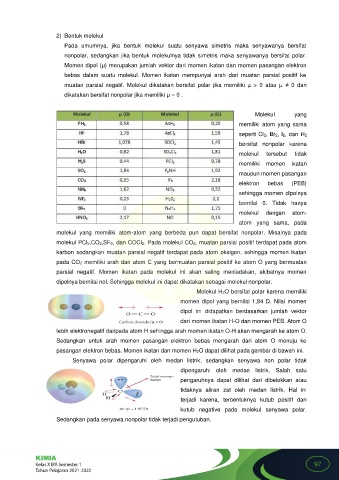
molekul PCl5,CO2,SF6, dan COCl2. Pada molekul CO2, muatan parsial positif terdapat pada atom
karbon sedangkan muatan parsial negatif terdapat pada atom oksigen, sehingga momen ikatan
pada CO2 memiliki arah dari atom C yang bermuatan parsial positif ke atom O yang bermuatan
parsial negatif. Momen ikatan pada molekul ini akan saling meniadakan, akibatnya momen
dipolnya bernilai nol. Sehingga molekul ini dapat dikatakan sebagai molekul nonpolar.
Molekul H2O bersifat polar karena memiliki
momen dipol yang bernilai 1,84 D. Nilai momen
dipol ini didapatkan berdasarkan jumlah vektor
dari momen ikatan H-O dan momen PEB. Atom O
lebih elektronegatif daripada atom H sehingga arah momen ikatan O-H akan mengarah ke atom O.
Sedangkan untuk arah momen pasangan elektron bebas mengarah dari atom O menuju ke
pasangan elektron bebas. Momen ikatan dan momen H2O dapat dilihat pada gambar di bawah ini.
Senyawa polar dipengaruhi oleh medan listrik, sedangkan senyawa non polar tidak
dipengaruhi oleh medan listrik. Salah satu
pengaruhnya dapat dilihat dari dibelokkan atau
tidaknya aliran zat oleh medan listrik. Hal ini
terjadi karena, terbentuknya kutub positif dan
kutub negative pada molekul senyawa polar.
Sedangkan pada senyawa nonpolar tidak terjadi pengutuban.
97