Page 97 - bingx
P. 97
tolakannya. Sehingga terjadi gaya tarik-menarik antar molekul. Inilah yang disebut gaya tarik-
menarik dipol-dipol. Gambar dibawah menunjukan proses terbentuknya gaya dipol-dipol.
Gaya dipol-dipol
Gambar 4.17 proses terbentuknya gaya dipol-dipol
Ikatan Hidrogen
Terdapat banyak unsur yang membentuk senyawa dengan hidrogen, disebut sebagai “hidrida”.
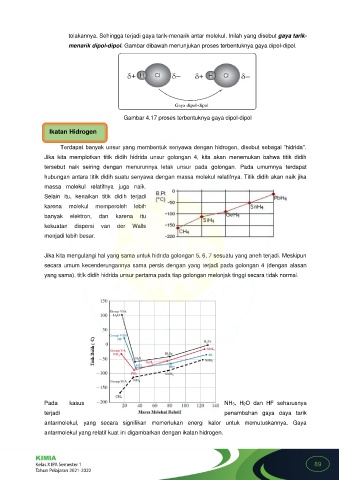
Jika kita memplotkan titik didih hidrida unsur golongan 4, kita akan menemukan bahwa titik didih
tersebut naik seiring dengan menurunnya letak unsur pada golongan. Pada umumnya terdapat
hubungan antara titik didih suatu senyawa dengan massa molekul relatifnya. Titik didih akan naik jika
massa molekul relatifnya juga naik.
Selain itu, kenaikan titik didih terjadi
karena molekul memperoleh lebih
banyak elektron, dan karena itu
kekuatan dispersi van der Walls
menjadi lebih besar.
Jika kita mengulangi hal yang sama untuk hidrida golongan 5, 6, 7 sesuatu yang aneh terjadi. Meskipun
secara umum kecenderungannya sama persis dengan yang terjadi pada golongan 4 (dengan alasan
yang sama), titik didih hidrida unsur pertama pada tiap golongan melonjak tinggi secara tidak normal.
Pada kasus NH3, H2O dan HF seharusnya
terjadi penambahan gaya daya tarik
antarmolekul, yang secara signifikan memerlukan energi kalor untuk memutuskannya. Gaya
antarmolekul yang relatif kuat ini digambarkan dengan ikatan hidrogen.
89